ヨーロッパ医薬品 受託研究機関(CRO) 市場規模
業界: Healthcareヨーロッパ医薬品 契約研究機関(CRO)市場動向が2033に予測
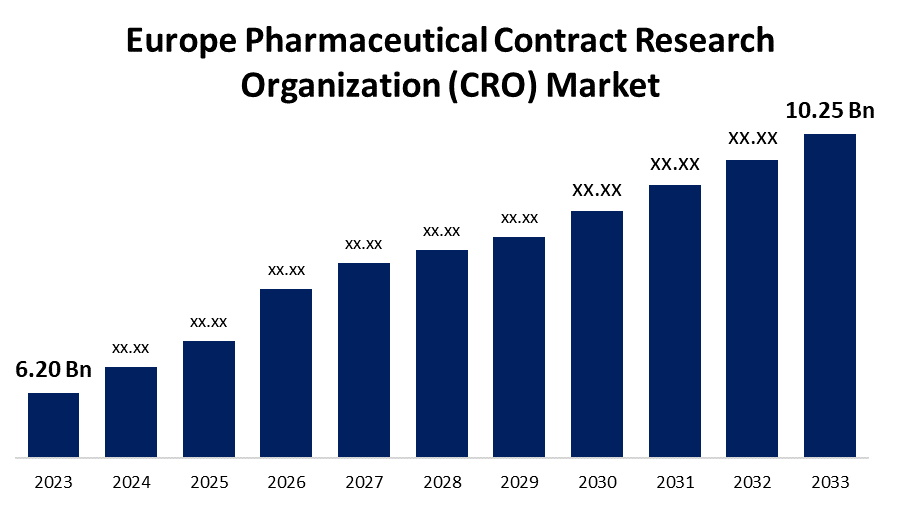
- 欧州医薬品受託研究機関(CRO)市場規模は2023年に米ドル6.20億で評価されました。
- 市場規模は2023年から2033年にかけて5.16%のCAGRで成長しています
- 欧州医薬品受託研究機関(CRO)市場規模は、2033年までにUSD 10.25億に達する見込み
このレポートの詳細については、こちらをご覧ください -
欧州医薬品受託研究機関(CRO)市場規模は、2033年までのUSD 10.25億ドルに達すると予想され、2023年から2033年までの1.46%のCAGRで成長しています。
市場概観
医薬品受託研究機構(CRO)は、製薬会社に研究開発(研究開発)サービスを提供する事業です。 CROは、医薬品開発プロセスに不可欠である臨床試験を監督し、実行するために契約されています。 企業は、臨床試験を管理するために必要とされる専門知識と経験のために、CROと共同作業することを選択します。 CROに対する臨床試験の責任をアウトソーシングすることで、他の重要な活動に集中しながら、時間とリソースを節約できます。 ヨーロッパでは、臨床試験の設計、患者の登録、サイトの監督、データ評価、規制ガイダンス、生物学的統計、医学的ライティング、薬局など、幅広いサービスを提供しています。 複数のグローバルクロスは、特定の治療分野や臨床試験の段階に焦点を当てる多くの地域の組織に加えて、ヨーロッパで大きな存在を持っています。 ドイツ、フランス、イギリス、スペイン、スイスなどの国は、臨床試験の主要拠点として認められています。 がん、アルツハイマー病、心臓病などの慢性疾患の高発生率で燃料を補給した欧州製薬のCRO市場は、欧州全域で急速に成長しています。 ヨーロッパは、科学的および臨床革新を生成し、進めるために堅牢な基盤を提供する多数の評判の良い研究機関、医療センターおよび病院に家です。
レポートカバレッジ
この研究報告では、欧州医薬品受託研究機関(CRO)の市場を様々な分野や地域に基づいて分類し、各サブマーケットにおける収益成長予測やトレンド分析を行っています。 本レポートでは、欧州医薬品受託研究機関(CRO)市場における主要な成長因子、機会、課題を分析しています。 市場展開や製品立ち上げ、開発、パートナーシップ、合併、買収などの競争戦略は、市場で競争力のある風景を描くために含まれています。 レポートは戦略的にキー市場プレーヤーを特定し、欧州製薬契約研究機関(CRO)市場の各サブセグメントでコアコンピテンシーを分析します。
ヨーロッパ医薬品 契約研究機関(CRO)市場 レポートの対象範囲
| レポートの対象範囲 | Details |
|---|---|
| 基準年: | 2023 |
| の市場規模 2023: | USD 6.20億 |
| 予測期間: | 2023-2033 |
| 予測期間のCAGR 2023-2033 : | 5.16% |
| 2033 価値の投影: | USD 10.25億円 |
| 過去のデータ: | 2019年10月20日 |
| ページ数: | 230 |
| 表、チャート、図: | 156 |
| 対象となるセグメント: | タイプによって、 サービス |
| 対象企業:: | IQVIA、世界的な臨床試験、Syneos Health、Medpace、Clinipace、WuXi AppTec、Almac、FGK臨床研究、CTI、およびその他の主要企業. |
| 落とし穴と課題: | COVID-19は、挑戦、未来、成長、及び分析を空にし、 |
このレポートの詳細については、こちらをご覧ください -
工場の運転
欧州製薬のCRO市場は、がんや心臓病などの慢性疾患の増大の蔓延によって主に駆動され、効果的な治療に対する高まっています。 同時に、製薬会社の間で成長している傾向は、コスト効率性によって動機付けられ、専門的知識へのアクセスを促す、クロスへの研究開発活動をアウトソーシングします。この傾向は、複雑な医薬品開発プロセスを処理する必要性と一緒に臨床試験の増加を含みます。 がん、糖尿病、心血管疾患を含む慢性疾患の増大率は、新しい治療法の選択肢に対する需要が高まっています。これにより、臨床試験や医薬品開発を管理するために、CROサービスの必要性が高まります。 製薬会社では、研究開発の業務を進んで、経費を削減し、専門的知識をタップし、医薬品開発のタイムラインを強化しています。 医薬品開発の複雑性が高まっています。特に、個人化された医薬品や標的療法のような領域では、高度な技術と専門性を装備し、臨床試験を専門的に管理する必要があります。
工場の修復
欧州製薬のCRO市場のためのいくつかの重要な妨げ要因は、熟練した人員、厳格な規制遵守、臨床試験に関連する高い費用、複雑な臨床試験設計、CRO間の激しい競争、データプライバシーに関する懸念、およびヨーロッパ全域のさまざまな国の規制をナビゲートする課題で構成されています。 これらの要因はすべて、運用効率とクロスのコストに影響を与えることによって市場成長を阻害する可能性があります。
市場区分
ヨーロッパ医薬品受託研究機関(CRO)市場シェアは、種類とサービスに分類されます。
- 予測期間を通じて最大の市場シェアを持たせることが期待されます。
ヨーロッパ医薬品受託研究機関(CRO)市場は、医薬品の発見、前臨床、臨床に分類されます。 これらの中で、予測期間を通じて最大の市場シェアを保持することが期待されます。 このセグメントの増加は、臨床試験、厳格な規制枠組み、患者中心的なアプローチへの移行のための増加の必要性に起因することができます。 受託研究機関(CRO)は、患者のエンゲージメントと保持を改善するための技術や方法論を採用しています。これにより、臨床分野におけるポジションをさらに強化します。
- 予測期間中、欧州医薬品受託研究機関(CRO)市場を廃止することが期待されます。
サービスに基づき、欧州医薬品受託研究機関(CRO)市場は、プロジェクト管理/臨床供給管理、データ管理、規制/医療業務、医療ライティング、臨床モニタリング、品質管理/品質保証、バイオ統計、その他に分けられます。 これらの中で、予測期間中、欧州医薬品受託研究機関(CRO)市場を廃止することが期待されます。 臨床モニタリングは、臨床試験の完全性と遵守を維持する上で重要な役割を果たします。 治験の実行を管理し、データの正確性を確認し、規制基準の遵守を確実にし、医薬品開発プロセスの重要な要素として機能します。
競争分析:
本レポートでは、欧州医薬品受託研究機関(CRO)市場に関与する主要な組織/企業戦略、セグメント市場シェア、およびSWOT分析を中心に、製品提供、事業概要、地理的存在感、企業戦略、セグメント市場シェアに関する比較評価を適切に提供しています。 また、製品開発、イノベーション、ジョイントベンチャー、パートナーシップ、合併、買収、戦略的アライアンス、その他を含む、企業の現在のニュースと開発に焦点を当てた実証分析も実施しています。 これにより、市場での全体的な競争の評価が可能になります。
主要企業リスト
- IQVIAの特長
- 世界的な臨床試験
- Syneos 健康
- メデパス
- クリニピス
- WuXiアプリテック
- アルマック
- FGK 臨床研究
- ログイン
- その他
主ターゲット聴衆
- マーケットプレイヤー
- IR情報
- エンドユーザー
- 政府の権限
- コンサルティング・リサーチファーム
- ベンチャーキャピタル
- 付加価値リセラー(VAR)
最近の開発
- 2024年3月、 Veedaの臨床研究リミテッドは、その成功した医薬品開発実績で知られる包括的な契約研究組織(CRO)であり、腫瘍学の分野における臨床試験を実施することに焦点を当てた個人的に所有されているヨーロッパCROのヘッドの買収を発表しました。
市場セグメント
この研究では、2020年から2033年までのヨーロッパ、地域、および国レベルでの収益を予測しています。 Spherical Insights は、欧州医薬品受託研究機構(CRO)市場を以下のセグメントに基づいてセグメント化しました。
ヨーロッパ医薬品 受託研究機関(CRO)市場、 タイプ別
- ドラッグディスカバリー
- プレ臨床
- 臨床検査
ヨーロッパ医薬品 受託研究機関(CRO)市場、 サービス
- プロジェクト管理/臨床供給管理
- データ管理
- 規制・医療関連
- 医療の執筆
- 臨床モニタリング
- 品質管理・保証
- バイオ統計学
- その他
このレポートを購入するにはサポートが必要ですか?